羥醛縮合反應----阿拉丁試劑

什么是羥醛縮合反應?
醛醇縮合反應是由Charles Wurtz提出的一種有機反應,他于1872年首次從乙醛中制備出β-羥基醛[1]。在醛醇縮合反應中,烯酸鹽離子與羰基化合物在酸/堿催化劑的存在下反應生成β-羥基醛或β-羥基酮,隨后脫水得到共軛的烯酮。是一種有效的碳-碳成鍵反應。醛醇縮合反應的基本步驟是:
1. 醛醇(醛+醇)反應-醛(或酮)烯酸酯與醛(或酮)的另一分子在NaOH或KOH存在下反應,形成β-羥基醛(或酮)。
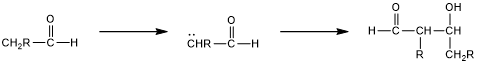
2. 脫水/消除反應——從β-羥基醛(或酮)中除去水分子,形成α,β-不飽和醛或α,β-不飽和酮。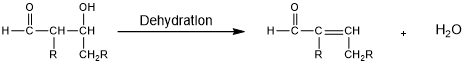
請參閱安全數據表,以了解有關危害和安全處理措施的信息。
應用場景
醛醇縮合反應可用于以下合成:
· 脂肪酸的酶促合成[2]
· 埃博霉素B的高效全合成[3]
· (E)-6-(2,2,3-三甲基-環戊-3-烯基)-己-4-烯-3-酮的制備[4]:
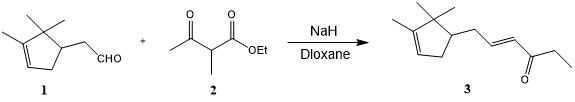
將2-甲基乙酰乙酸乙酯(2)(727 mg, 4.53 mmol)添加至NaH (184 mg, 4.60 mmol)存于二氧六環(25 mL)中之攪拌溶液中。然后添加莰烯醛(1)(707 mg, 3.72 mmol)并將混合物回流15 h。然后添加2N HCl (15 mL)并用Et2O (3×15 mL)萃取混合物。用2N HCl (2×15 mL)、飽和Na2CO3 (2×15 mL)和鹽水(3×15 mL)洗滌合并的有機層。經無水Na2SO4干燥有機相并且在減壓下蒸發溶劑,得到殘余物(900 mg),在減壓下通過蒸餾純化殘余物,得到標題化合物3 (505 mg, 2.63 mmol, 58%)。
· 聚戊二醛高聚物的合成[5]
· (±)- 麻 黃 堿的立體選擇性合成[6]
· 大環內酯類和離子載體抗生素(天然產物)的合成[7]
· 兩種結構獨特的四環喹諾酮類化合物——雙螺旋胺A和B的全合成[8]
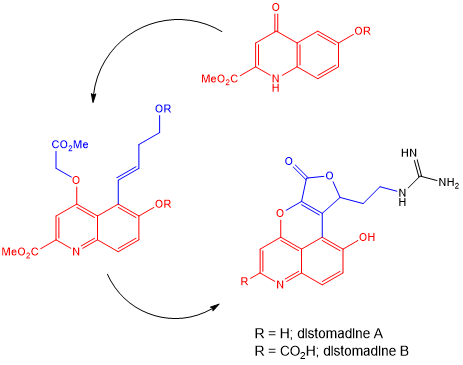
該路線分為三步,通過5-溴-4-甲氧基羰基甲氧基喹啉與乙烯基硼酸酯的Suzuki交叉偶聯,然后進行α-酮羥基化和分子內醛醇縮合和內酯化的雙環化,從而獲得吡喹喹啉丁烯內酯環。隨后通過對側鏈的操作,引入胍片段,完成了雙螺旋胺B的合成,而雙螺旋胺A的同系物是由后期中間體脫羧作用得到的。
最 新研究及未來發展趨勢
· 采用水溶性杯芳烴作為反相轉移催化劑,對活化的甲基和亞甲基化合物進行了醛縮合和邁克爾加成反應[9]
· 采用含銫離子催化劑,在SBA-15介孔分子載體上進行乙酸甲酯與甲醛的縮合反應[10]
該催化劑在縮合反應中表現出較高的催化活性。XRD表征表明,低于5 wt%負載的硝酸銫在SBA-15支架上高度分散。FT-IR和XPS結果證實催化劑表面形成Si-O-Cs。NH3-TPD和CO2-TPD結果表明,弱Lewis酸堿對負載在表面,這些弱酸堿活性位點可能有利于醛醇縮合反應。5Cs/SBA-15催化劑表現出最 高的乙酸甲酯轉化率(48.4%)和95.0%的丙烯酸甲酯選擇性。失活催化劑經煅燒完全再生。催化劑再生9次,總操作時間超過60 h,乙酸甲酯的初始轉化率和對丙烯酸甲酯的選擇性均未發生變化。催化劑具有較高的催化活性,主要是由于載體表面的Si-O-Cs基團具有較強的弱酸堿性質。
· 環己酮與對硝基苯甲醛在水中的有機催化不對稱醛醇反應[11]
· 一鍋法銅催化醚化/醛醇縮合級聯反應制備二苯并西平內酰胺[12]
· 通過烷基化、區域選擇性碘化、醛醇縮合、Suzuki偶聯和[1,3]-sigma重排等方法合成一系列二戊烯化和二癸基化查爾酮類似物[13]
· 在KOH存在的甲醇溶劑中,苊醌與苯乙酮進行邁克爾加成和醛醇縮合,可形成多米諾骨牌序列,從而進一步形成了不同的2:2加合物[14]
· 縮醛反應通常會利用酸性或堿性催化劑進行,因此,MCM-41的改性是通過兩個酸性基團(3-丙基磺基、3-丙基羧基)和一個堿性基團(3-(1,2-二乙基氨基)丙基)后接枝法實現的,采用的是經硫酸和硝酸處理的MCM-41[15]。用BET、元素分析和UV-Vis光譜對所制備的功能化材料進行了表征。結果表明,最 佳反應條件為反應混合物溫度100℃,反應物4-異丙基苯甲醛:丙醛的摩爾比為1:2,催化劑的用量和種類為50 wt%的MCM SO3H(與4-異丙基苯甲醛的用量相比),丙醛的加入時間為90分鐘,反應的適宜溶劑為甲苯。在最 佳反應條件下,甲醛的收率為45%。將所得結果與H2SO4均相催化的效果進行了比較,其收率為15%。
參考文獻
1. Nielsen AT, Houlihan WJ. The Aldol Condensation. 1-438. https://doi.org/10.1002/0471264180.or016.01
2. Brady RO. 1958. The Enzymatic Synthesis of Fatty Acids by Aldol Condensation. Proceedings of the National Academy of Sciences. 44(10):993-998. https://doi.org/10.1073/pnas.44.10.993
3. Balog A, Haris C, Savin K, Zhang X, Chou T, Danishefsky S. 1998. Angew. Chem. Int. Ed.. 372675.
4. Badía C, Castro J, Linares Palomino P, Salido S, Altarejos J, Nogueras M, Sánchez A. (E)-6-(2,2,3-Trimethyl-cyclopent-3-enyl)-hex-4-en-3 one. Molbank. 2004(1): M388. https://doi.org/10.3390/m388
5. Tashima T, Imai M, Kuroda Y, Yagi S, Nakagawa T. 1991. Structure of a new oligomer of glutaraldehyde produced by aldol condensation reaction. J. Org. Chem.. 56(2):694-697. https://doi.org/10.1021/jo00002a038
6. Heathcock CH, Buse CT, Kleschick WA, Pirrung MC, Sohn JE, Lampe J. 1980. Acyclic stereoselection. 7. Stereoselective synthesis of 2-alkyl-3-hydroxy carbonyl compounds by aldol condensation. J. Org. Chem.. 45(6):1066-1081. https://doi.org/10.1021/jo01294a030
7. Masamune S, Choy W, Kerdesky Francis A. J., Imperiali B. 1981. Stereoselective aldol condensation. Use of chiral boron enolates. J. Am. Chem. Soc.. 103(6):1566-1568. https://doi.org/10.1021/ja00396a050
8. Jolibois AER, Lewis W, Moody CJ. 2014. Total Synthesis of (±)-Distomadines A and B. Org. Lett.. 16(4):1064-1067. https://doi.org/10.1021/ol403598k
9. Shimizu S, Shirakawa S, Suzuki T, Sasaki Y. 2001. Water-soluble calixarenes as new inverse phase-transfer catalysts. Their application to aldol-type condensation and Michael addition reactions in water. Tetrahedron. 57(29):6169-6173. https://doi.org/10.1016/s0040-4020(01)00572-5
10. Yan J, Zhang C, Ning C, Tang Y, Zhang Y, Chen L, Gao S, Wang Z, Zhang W. 2015. Vapor phase condensation of methyl acetate with formaldehyde to preparing methyl acrylate over cesium supported SBA-15 catalyst. Journal of Industrial and Engineering Chemistry. 25344-351. https://doi.org/10.1016/j.jiec.2014.11.014
11. Mase N, Nakai Y, Ohara N, Yoda H, Takabe K, Tanaka F, Barbas CF. 2006. Organocatalytic Direct Asymmetric Aldol Reactions in Water. J. Am. Chem. Soc.. 128(3):734-735. https://doi.org/10.1021/ja0573312
12. Lim HS, Choi YL, Heo J. 2013. Synthesis of Dibenzoxepine Lactams via a Cu-Catalyzed One-Pot Etherification/Aldol Condensation Cascade Reaction: Application toward the Total Synthesis of Aristoyagonine. Org. Lett.. 15(18):4718-4721. https://doi.org/10.1021/ol402036t
13. Wang H, Zhang L, Liu J, Yang Z, Zhao H, Yang Y, Shen D, Lu K, Fan Z, Yao Q, et al. 2015. Synthesis and anti-cancer activity evaluation of novel prenylated and geranylated chalcone natural products and their analogs. European Journal of Medicinal Chemistry. 92439-448. https://doi.org/10.1016/j.ejmech.2015.01.007
14. Domino reaction sequences leading to the formation of 2:2 adducts between acenaphthenequinone and acetophenone. 2014(6):127. https://doi.org/10.3998/ark.5550190.p008.834
15. Vrbková E, Vyskocilová E, Cerveny L. 2015. Functionalized MCM-41 as a catalyst for the aldol condensation of 4-isopropylbenzaldehyde and propanal. Reac Kinet Mech Cat. 114(2):675-684. https://doi.org/10.1007/s11144-014-0811-2
阿拉丁提供相關產品:
產品貨號 | 產品名稱 |
C106972 | 1,3-環己二酮 ,97% |
B104602 | 2,3-丁二酮 ,standard for GC,≥99.0%(GC) |
B104601 | 2,3-丁二酮 ,98% |
B104603 | 2,3-丁二酮 ,分析標準品,≥99.0%(GC) |
H106696 | 2,3-己二酮 ,90% |
P106293 | 2,3-戊二酮 ,98% |
C139450 | 2-環戊烯-1-酮 ,≥96.0%(GC) |
C352403 | 2-環戊烯-1-酮縮乙醛 ,97% |
C107526 | 2-環戊基環戊酮 ,97% |
H103803 | 2-庚酮 ,98% |
H103827 | 2-庚酮 ,分析標準品,≥99.8%(GC) |
H105744 | 2-己酮 ,98% |
H105743 | 2-己酮 ,standard for GC,>99.5%(GC) |
H117489 | 2-己基環戊酮 ,≥96%(GC) |
P103783 | 2-戊酮 ,色譜級,99.0% |
P103782 | 2-戊酮 ,分析標準品,用于環境分析,≥99.8%(GC) |
H117488 | 2-庚基環戊酮 ,>99.0%(GC) |
A106311 | 乙醛 ,99.5% |
B110460 | 苯甲醛 ,AR,≥98%(GC) |
B103861 | 二苯甲酮 ,99% |
B103860 | 二苯甲酮 ,CP |
C105368 | 氯化銫 ,AR,≥99% |
C108569 | 環戊酮 ,分析標準品 |
D105295 | 十二烷基三甲基氯化銨(DTAC) ,99% |
H157071 | 六氨基氯化鈷 ,>99.0%(T) |
H105309 | 十六烷基三甲基氯化銨(CTAC) ,97% |
L108933 | 溴化鋰溶液 ,55 wt. % in H2O |
L101684 | 碳酸鋰 ,99.99% metals basis |
L298760 | 氯化鋰 ,無水級,98% |
N108314 | 氧化鎳 ,AR,99.0 % |
P165286 | 丙酮酸 ,≥70% |
R109233 | 三氯化銠(III) 水合物 ,Rh 38.5-42.5% |
S111733 | 無水碳酸鈉 ,GR,≥99.8% |
S110860 | 氫化鈉 ,60% dispersion in mineral oil |
S140966 | 高氯酸鈉,無水(易制爆) ,99% |
S105271 | 高氯酸鈉,無水(易制爆) ,色譜級,99.0% |
T103857 | 三氧化鎢 ,99.8% metals basis |
Z112532 | 氯化鋅 ,99.95% metals basis |
H399657 | 鹽酸(易制毒) ,37% |
B131582 | 2-溴苯乙酮 ,用于GC衍生化, ≥99.0% |
標簽:羥醛縮合反應
全部評論(0條)
推薦閱讀
-

- 羥醛縮合反應----阿拉丁試劑
- 什么是羥醛縮合反應? 醛醇縮合反應是由Charles Wurtz提出的一種有機反應,他于1872年首次從乙醛中制備出β-羥基醛[1]。
-

- Knoevenagel縮合反應 ----阿拉丁試劑
- 有機化學是一個廣闊的領域,包括生產復雜分子的各種合成途徑。其中一種方法是Knoevenagel縮合反應。這是一種多用途的反應,涉及羰基化合物和活性亞甲基化合物的縮合,形成α,β-不飽和羰基化合物。
-

- Heck反應----阿拉丁試劑
- Heck反應是有機化學中最為廣泛使用的碳-碳偶聯反應之一。Heck反應是烯烴與芳基或乙烯基鹵化物(或三氟甲磺酸酯)用于合成取代烯烴的鈀催化交叉偶聯反應。
-

- Diels-Alder反應----阿拉丁試劑
- Diels-Alder反應----阿拉丁試劑
-

- 傅-克酰基化反應----阿拉丁試劑
- 傅-克酰基化反應是指一類在路易斯酸作為催化劑的條件下,芳烴與酰氯或酸酐進行酰化的反應。
-
- 酸胺縮合搞不定,試試Mukaiyama試劑:一個非常高效廣譜的縮合試劑
- 進公司做的第一個反應就是酸胺縮合,這類反應說簡單簡單,說難有的反應還是有難度的。常規的酸胺縮合,使用HATU,T3P,EDCI等都可以很好地進行,只要你原料沒有漏加,基本上都能成功。然而,有的反應,比如惰性的親核胺,或大位阻的羧酸參與的酸胺縮合往往需要特別的高活性的縮合試劑參與。今天小編給大家介紹一
-

- Fries重排----阿拉丁試劑
- Fries重排反應是指在路易斯酸或布朗斯特酸( 如HF、AlCl3, BF3, TiCl4, 或 SnCl4)催化下,以酚酯作為原料重排合成鄰位或對位酰基酚的反應[1]。
-

- 免疫沉淀技術----阿拉丁試劑
- 免疫沉淀(IP)是應用最廣泛的免疫化學技術之一。
-

- 蛋白樣品制備流程----阿拉丁試劑
- 蛋白分析的第一步是蛋白提取,蛋白提取方法包括化學抽提法、物理抽提法和生物學抽提法。蛋白提取無論通過機械處理還是基于去垢劑的提取方法,都會不可避免地破壞細胞穩態,導致蛋白降解或不穩定。
-

- 代謝信號通路----阿拉丁試劑
- 細胞內穩態是由幾個關鍵代謝途徑的協調活動調節。這些過程包括碳水化合物代謝、脂質代謝、谷氨酰胺代謝和核苷酸代謝,它們維持細胞的能量狀態,并提供必要的成分以確保細胞正常功能。
-
- 白蛋白的應用----阿拉丁試劑
- 白蛋白是人體血漿中最主要的蛋白質,對維持血容量和體液平衡有重要作用。它是一種溶于水且遇熱凝固的球形單純蛋白,分子結構于1975年闡明,其為含585個氨基酸殘基的單鏈多肽,分子形狀呈橢圓形。
-

- 生物緩沖液選擇指南----阿拉丁試劑
- 生物緩沖液選擇指南----阿拉丁試劑
-

- DNA損傷和修復----阿拉丁試劑
- 細胞DNA的損傷與突變和癌癥的發生有關。人類細胞中的DNA每天要經歷數千到數百萬次的破壞事件,這些事件是由外部(外源性)和內部代謝(內源性)過程產生的。
-

- 關于催化劑的基本概念----阿拉丁試劑
- 過渡態理論,也稱活化復合體理論或絕對反應速率理論,是對化學反應和其他過程的研究,認為它們是通過組成原子和分子的相對位置和勢能的連續變化來進行的。
-

- 納米材料的化學合成方法----阿拉丁試劑
- 任何納米材料合成方法的目標都是創造一種材料,這種材料由于其長度范圍在 1-100納米之間而獲得性能。因此,合成方法應該在這個范圍內表現出尺寸控制, 這樣才能獲得新的性質。納米材料的合成和納米結構的制備
-

- 卡爾費休法的應用范圍----阿拉丁試劑
- 卡爾費休法可用于廣泛的物質。然而,該方法依賴于卡爾費休試劑和水之間反應的碘量測定。因此,如果樣品包含與碘單質反應的物質,結果將會出現正誤差,如果樣品包含通過氧化碘化合物產生碘單質的物質,結果將顯示負誤
①本文由儀器網入駐的作者或注冊的會員撰寫并發布,觀點僅代表作者本人,不代表儀器網立場。若內容侵犯到您的合法權益,請及時告訴,我們立即通知作者,并馬上刪除。
②凡本網注明"來源:儀器網"的所有作品,版權均屬于儀器網,轉載時須經本網同意,并請注明儀器網(www.ghhbs.com.cn)。
③本網轉載并注明來源的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點或證實其內容的真實性,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品來源,并自負版權等法律責任。
④若本站內容侵犯到您的合法權益,請及時告訴,我們馬上修改或刪除。郵箱:hezou_yiqi















參與評論
登錄后參與評論