
- 2025-04-25 14:14:59全彩調(diào)控
- 全彩調(diào)控是一種先進的顯示技術(shù),它通過對紅、綠、藍三原色的精細調(diào)節(jié),實現(xiàn)色彩的精準控制和豐富呈現(xiàn)。這種技術(shù)廣泛應(yīng)用于高端顯示設(shè)備中,如LED顯示屏、OLED電視等,能夠展現(xiàn)出更加逼真、細膩的色彩效果。通過全彩調(diào)控,用戶可以享受到更加真實、飽滿的視覺體驗,滿足對色彩精度和畫面質(zhì)量的高要求。
資源:397個 瀏覽:2次展開
全彩調(diào)控相關(guān)內(nèi)容
全彩調(diào)控文章
-
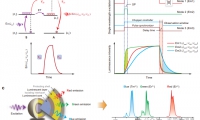
- 全彩防偽新方案!卓立漢光光譜儀助力單波長激發(fā)納米顆粒多色切換
- 華南理工大學(xué)周博教授及其合作單位提出全新的概念模型,即在單一980nm激光激發(fā)下,實現(xiàn)多層核殼納米顆粒全彩調(diào)控,為發(fā)光材料設(shè)計和前沿光子應(yīng)用開辟新方向。
全彩調(diào)控產(chǎn)品
產(chǎn)品名稱
所在地
價格
供應(yīng)商
咨詢

- 全彩3D打印機
- 國外 亞洲
- 面議
-
上海錦廷機電科技有限公司
售全國
- 我要詢價 聯(lián)系方式

- 小型全彩3D打印機
- 國外 亞洲
- 面議
-
上海錦廷機電科技有限公司
售全國
- 我要詢價 聯(lián)系方式

- 廣皓天霉菌培養(yǎng)箱溫濕度調(diào)控箱
- 國內(nèi) 廣東
- ¥81600
-
廣東皓天檢測儀器有限公司
售全國
- 我要詢價 聯(lián)系方式

- 北京索斯克手持雙目微光全彩夜視儀
- 國內(nèi) 北京
- 面議
-
北京索斯克科技開發(fā)有限公司
售全國
- 我要詢價 聯(lián)系方式

- GMS150高精度氣體調(diào)控系統(tǒng)
- 國外 歐洲
- 面議
-
北京易科泰生態(tài)技術(shù)有限公司
售全國
- 我要詢價 聯(lián)系方式
全彩調(diào)控問答
- 2022-10-31 15:28:07神經(jīng)調(diào)控中,如何特異性激活某一類型神經(jīng)元?
100人看過
- 2022-07-13 15:10:55Neuron:脊髓神經(jīng)元調(diào)控傷害性熱刺激感受新機制
- 帶你看文獻,只做純干貨文獻精讀第25期文章概述對人來說,皮膚溫度高于43℃會引起急性疼痛,長時間暴露于傷害性熱刺激中會造成組織損傷,并破壞體溫的動態(tài)平衡。脊髓背角神經(jīng)元在處理和傳遞來自背根神經(jīng)節(jié)(Dorsal Root Ganglion, DRG)痛覺傳入纖維的感覺信號中起著關(guān)鍵作用,但是,傷害性熱刺激信號在脊髓中的處理過程尚不清楚。2022年5月12日,美國凱斯西儲大學(xué)醫(yī)學(xué)院的研究人員在《Neuron》雜志上發(fā)表題為“A novel spinal neuron connection for heat sensation”的文章,該研究證實了由脊髓ErbB4+(ErbB4,一種表皮生長因子受體家族的酪氨酸激酶受體)神經(jīng)元能夠通過NRG1-ErbB4信號通路來調(diào)控機體對傷害性熱刺激的感受,揭示了脊髓中一個新的傷害性熱刺激感受的調(diào)控機制。核心觀點1、脊髓ErbB4+神經(jīng)元能夠被傷害性熱刺激所激活;2、脊髓ErbB4+神經(jīng)元受TRPV1+傷害感受器的單突觸神經(jīng)支配;3、消融或抑制ErbB4+神經(jīng)元會降低動物對傷害性熱刺激的感受;4、同時抑制脊髓中ErbB4+、SST+和CCK+神經(jīng)元能夠進一步降低傷害性熱刺激的感受;5、NRG1-ErbB4信號通路能夠促進傷害性熱刺激的感受和熱痛過敏反應(yīng)。研究結(jié)果分析1. 傷害性熱刺激能夠激活脊髓中ErbB4+興奮性神經(jīng)元為了識別對傷害性熱刺激產(chǎn)生反應(yīng)的神經(jīng)元,作者利用了EGFP表達依賴于內(nèi)源性cFos啟動子的cFos::shEGFP小鼠。當(dāng)cFos::shEGFP小鼠受到傷害性熱刺激(52℃熱板)時,脊髓背角神經(jīng)元中的shEGFP表達增加,大量的shEGFP+神經(jīng)元位于脊髓背角表層(Ⅰ~Ⅱ?qū)樱@是傷害性感覺信息的接收區(qū)域。單細胞RT-PCR結(jié)果顯示,78%的shEGFP+神經(jīng)元為興奮性神經(jīng)元(Vglut2+),22%的shEGFP+神經(jīng)元為GABA能神經(jīng)元(GAD65/67+)。這與之前的研究結(jié)果一致,即大多數(shù)對傷害性熱刺激產(chǎn)生反應(yīng)的神經(jīng)元是興奮性神經(jīng)元。然而,shEGFP+神經(jīng)元具有極高的異質(zhì)性,涉及到多種類型的神經(jīng)元,比如,其中膽囊收縮素陽性(Cholecystokinin+, CCK+)和生長激素抑制素陽性(Somatostatin+, SST+)神經(jīng)元分別占18%和14%。值得注意的是,~1/3的shEGFP+神經(jīng)元表達了ErbB4,而ErbB4主要表達于興奮性神經(jīng)元中。這些結(jié)果表明,傷害性熱刺激能夠激活一群ErbB4+興奮性神經(jīng)元。為了驗證這一假設(shè),作者對ErbB4:: CreER;Ai9小鼠進行熱刺激,該小鼠tdTomato的表達依賴于內(nèi)源性的ErbB4啟動子。在脊髓中,ErbB4-tdT+神經(jīng)元主要集中在背角,分布于多層背角和脊髓外側(cè)核(Lateral Spinal Nucleus, LSN)中,然而,熱激活的ErbB4-tdT神經(jīng)元(cFos+)主要位于脊髓背角表層中。ErbB4-tdT神經(jīng)元約占cFos+神經(jīng)元33%。這些結(jié)果確認了脊髓背角表層ErbB4+興奮性神經(jīng)元是一種新型的傷害性熱反應(yīng)細胞。2. 脊髓ErbB4+,SST+和CCK+神經(jīng)元負責(zé)傷害性熱刺激感受接下來,作者通過在ErbB4::CreER;LSL-EYFP(ErbB4-EYFP)小鼠椎管內(nèi)注射AAV-mCherry-DIO-dtA(AAV-dtA)病毒,在ErbB4+細胞中特異性的表達A型白喉毒素(diphtheria toxin subunit A, dtA)來消融脊髓中的ErbB4+神經(jīng)元。與注射對照病毒的小鼠相比,注射AAV-dtA的ErbB4-EYFP小鼠中EYFP+細胞和Nmur2+神經(jīng)元數(shù)目顯著減少。接下來,小鼠接受了一系列的行為測試。與對照小鼠相比,注射AAV-dtA的ErbB4-EYFP小鼠在熱板以及哈格里夫斯實驗中,后爪退縮和舔爪的潛伏期中增加了~40%,表明ErbB4+神經(jīng)元對傷害性熱刺激的感受至關(guān)重要。辣椒素能夠激活感覺神經(jīng)元中的TRPV1受體,誘發(fā)自發(fā)性疼痛,與對照組相比,在AAV-dtA注射的ErbB4-EYFP小鼠,辣椒素誘導(dǎo)的小鼠舔足次數(shù)減少了30%。這些結(jié)果表明,ErbB4+神經(jīng)元是傷害性熱刺激的感受所必需的。此外,注射AAV-dtA的ErbB4-EYFP小鼠對機械刺激、冰冷-溫?zé)帷⒁约鞍W刺激的反應(yīng)與對照類似。這表明脊髓ErbB4+神經(jīng)元可能不參與這些刺激的感受。除了ErbB4+神經(jīng)元,SST+和CCK+中間神經(jīng)元也會被傷害性熱刺激激活。為了確定它們對熱刺激感受的貢獻,作者分別消融了這些神經(jīng)元。在熱板以及哈格里夫斯實驗中,消融SST+神經(jīng)元后小鼠的反應(yīng)潛伏期分別增加了26%和22%,而消融CCK+神經(jīng)元的反應(yīng)潛伏期則沒有增加。值得注意的是,將ErbB4+、SST+和CCK+三類神經(jīng)元同時消融時,小鼠對傷害性熱刺激感受的抑制作用顯著增加到60% - 80%。這些結(jié)果表明,傷害性熱刺激感受涉及脊髓中的ErbB4+、SST+和CCK+神經(jīng)元。3. ErbB4+神經(jīng)元受TRPV1+痛覺感受器的單突觸神經(jīng)支配,且能被傷害性熱刺激而非機械刺激所激活不同的軀體感覺信息由不同類型的傳入纖維傳入脊髓背角:Aβ纖維主要用于傳遞非傷害性刺激,而Aδ和C纖維用于傳遞傷害性刺激。為了確定ErbB4+神經(jīng)元的信息來源,作者利用帶背根的縱向脊髓切片來記錄背角中ErbB4+神經(jīng)元的興奮性突觸后電流(EPSCs)。對于Aδ和C纖維的刺激傳入,分別有76%和54%的表層ErbB4+神經(jīng)元記錄到了EPSCs,其中67%和46%的ErbB4+神經(jīng)元為單突觸傳入。相比之下,表層中有25%的ErbB4+神經(jīng)元記錄到Aβ纖維信息傳入,只有9.1%是單突觸傳入。此外,在深層ErbB4+神經(jīng)元中,6.7%和5.6%的神經(jīng)元接受Aδ和C纖維的單突觸傳入。這些結(jié)果表明,淺表層的ErbB4+神經(jīng)元主要接受攜帶傷害性信息的C和Aδ纖維的單突觸傳入。為了驗證ErbB4+神經(jīng)元是否被TRPV1+傷害性感受器的突觸支配,作者用到了QX-314(一種細胞內(nèi)鈉通道抑制劑,其細胞進入依賴于TRPV1的激活)。單獨使用QX-314對C纖維傳入的ErbB4+神經(jīng)元EPSC振幅影響不大。然而,在TRPV1激活物辣椒素存在的情況下,QX-314使EPSCs減弱,表明ErbB4+神經(jīng)元接受TRPV1+纖維的支配。與之一致的是,在QX-314和辣椒素的存在下,對C纖維刺激有反應(yīng)的ErbB4+神經(jīng)元的數(shù)量減少了。這種作用是C纖維特異性的,因為A纖維中TRPV1表達較低,QX-314對刺激A纖維產(chǎn)生的EPSCs的影響不大。這些結(jié)果為表層ErbB4+神經(jīng)元受TRPV1+ C纖維的支配提供了藥理學(xué)依據(jù)。為了找到這種神經(jīng)支配的形態(tài)學(xué)證據(jù),作者將AAV-DIO-mCherry注射到TRPV1::Cre;ErbB4::CreER小鼠脊髓腰膨大區(qū)標(biāo)記ErbB4+神經(jīng)元,并將AAV-DIO-ChR2-EYFP注射到DRG中標(biāo)記TRPV1+末端。脊髓切片用突觸后標(biāo)記物Homer進行染色標(biāo)記。可以看到ErbB4+神經(jīng)元(mCherry+)被TRPV1+末端(即EYFP+)包圍。TRPV1+末端與Homer+突觸以及ErbB4+細胞密切相關(guān)。這些結(jié)果進一步表明,脊髓背角表層ErbB4+神經(jīng)元受到DRG中TRPV1+ 傳入纖維的支配。為了證明這些突觸是有功能的,作者利用光遺傳學(xué)激活表達視蛋白ChR2的TRPV1+末端。42%的表層ErbB4+神經(jīng)元能夠在光刺激下誘發(fā)EPSCs,這些EPSCs被TTX所抑制,而在TTX和4-AP同時存在的情況下,仍有36%的ErbB4+表層神經(jīng)元能夠被光刺激誘發(fā)EPSCs,這表明它們是由DRG中TRPV1+傳入纖維的單突觸所支配的。綜上所述,脊髓背角表層ErbB4+神經(jīng)元直接受TRPV1+傷害性感受器的單突觸神經(jīng)支配。為了確定ErbB4+神經(jīng)元是否對機械刺激產(chǎn)生反應(yīng),作者將AAV-DIO-ChR2-EYFP注射到MrgprD::CreER;ErbB4::CreER小鼠DRG中,讓傳導(dǎo)機械刺激的MrgprD+神經(jīng)元表達ChR2,同時將AAV-DIO-mCherry注射到腰膨大來標(biāo)記ErbB4+神經(jīng)元。然而,對脊髓切片進行光刺激,大多數(shù)的ErbB4+神經(jīng)元(87%)未能記錄到EPSCs,這表明大多數(shù)ErbB4+神經(jīng)元不接受來自機械刺激感覺神經(jīng)元的傳入。在3個響應(yīng)ErbB4+神經(jīng)元中,有2個被TTX和4-AP抑制,表明它們接受了多級突觸傳導(dǎo),只有一個出現(xiàn)了4-AP增強的EPSCs,表明其受到機械感覺神經(jīng)元的單突觸支配。作為對照,作者采用了相同的策略來觀察SST+脊髓神經(jīng)元對機械感覺神經(jīng)元刺激的反應(yīng)。大多數(shù)記錄的SST+神經(jīng)元(72%)產(chǎn)生了光刺激誘導(dǎo)的EPSCs,表明它們接受MrgprD+機械感覺神經(jīng)元的傳入,且61%為單突觸支配。這些結(jié)果表明,脊髓背角表層ErbB4+神經(jīng)元主要受傷害性熱刺激感受神經(jīng)元的支配,而非機械刺激感覺神經(jīng)元的支配。為了進一步表征在更接近生理條件下ErbB4+神經(jīng)元的敏感性,作者構(gòu)建了半完整的離體檢測范式,通過分離相連的部分脊髓、腰椎根、DRG、隱神經(jīng)和后肢皮膚,來記錄脊髓ErbB4+神經(jīng)元對皮膚刺激的反應(yīng)。在記錄的16個ErbB4+神經(jīng)元中,有9個(56%)對52℃刺激有反應(yīng),有5個(30%)對0℃刺激有反應(yīng)。對15℃和40℃刺激有反應(yīng)的神經(jīng)元分別為1個(7%)和2個(13%)。這些結(jié)果表明,表層ErbB4+神經(jīng)元對傷害性熱刺激的反應(yīng)較好,其次是冰冷刺激,而對涼或溫?zé)岽碳さ姆磻?yīng)較弱。為了確定ErbB4+神經(jīng)元是否對機械刺激有反應(yīng),研究者用Von-Frey絲刺激皮膚。在16個記錄的神經(jīng)元中,有14個無反應(yīng)。這些結(jié)果表明,脊髓背角表層ErbB4+神經(jīng)元對傷害性熱刺激比機械刺激更敏感。4.抑制ErbB4+神經(jīng)元會減弱動物對傷害性熱刺激的感受,反之則增強動物對熱刺激的感受隨后,作者探討了脊髓ErbB4+神經(jīng)元活性對傷害性熱刺激感受的影響。為了降低ErbB4+神經(jīng)元的活性,作者將AAV-DIO-hM4Di-mCherry(AAV-hM4Di)注射到ErbB4::CreER小鼠的脊髓腰膨大,并通過CNO來抑制ErbB4+神經(jīng)元活性。與對照相比,抑制ErbB4+神經(jīng)元增加了小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期,并減少了辣椒素誘導(dǎo)的舔足。抑制SST+而非CCK+神經(jīng)元,小鼠在熱板以及哈格里夫斯實驗中的反應(yīng)潛伏期增加,但對辣椒素誘導(dǎo)的舔足沒有影響。值得注意的是,當(dāng)這三類的神經(jīng)元活性同時降低時,小鼠對傷害性熱刺激感受的抑制效果增加60%~80%。這些結(jié)果表明脊髓ErbB4+、SST+和CCK+神經(jīng)元的活動共同參與傷害性熱刺激感受,支持群體編碼模式理論。為了增加脊髓ErbB4+神經(jīng)元的活性,作者將AAV-DIO-hM3Dq-mCherry注射到ErbB4::CreER小鼠的脊髓腰膨大。與對照相比,激活ErbB4+神經(jīng)元降低了小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期,且增加了辣椒素誘導(dǎo)的持續(xù)舔足時間。表明, ErbB4+神經(jīng)元激活增強了動物對傷害性熱刺激的感受。總之,這些結(jié)果揭示了ErbB4+神經(jīng)元在傷害性熱刺激感受中的關(guān)鍵作用。5. 傷害性熱刺激的感受依賴ErbB4激酶的活性ErbB4由生長因子神經(jīng)調(diào)節(jié)蛋白1(Neuregulin 1, NRG1)所激活,為了檢測NRG1-ErbB4信號通路是否參與了傷害性熱感受,作者檢測了脊髓背角NRG1和pErbB4的表達。結(jié)果顯示,暴露于52℃熱板的小鼠其脊髓背角NRG1和pErbB4的表達增加,表明傷害性熱刺激可以增強脊髓背角的NRG1-ErbB4信號。接下來,作者評估了 ErbB4的存在對傷害性熱刺激的感受是否必要,為此,作者構(gòu)建了ErbB4-rKO小鼠(該小鼠在除心臟外的任何組織,包括脊髓中都不表達ErbB4)。值得注意的是,與對照組小鼠相比,ErbB4-rKO小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期增加,且辣椒素誘導(dǎo)的舔足次數(shù)減少,表明ErbB4在這些反應(yīng)中發(fā)揮了作用。隨后,為了消除其它組織中ErbB4突變可能存在的影響,作者通過在ErbB4f/f小鼠脊髓腰膨大注射了AAV-Cre-GFP病毒,來特異性的敲除脊髓背角中的ErbB4。與對照組相比,脊髓背角ErbB4敲除使得小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期增加,辣椒素誘導(dǎo)的舔足次數(shù)減少。這些結(jié)果揭示了ErbB4在傷害性熱刺激感受中的必要作用。為了確定熱感受是否涉及ErbB4的激酶活性激活,作者以鞘內(nèi)注射的方式給小鼠注射阿法替尼(一種ErbB激酶抑制劑)。阿法替尼顯著減少了脊髓腰膨大中pErbB4的表達。動物在熱板、哈格里夫斯和辣椒素實驗中的反應(yīng)也減弱,但對針刺、掐和Von-Frey絲刺激反應(yīng)的影響不大。這些結(jié)果提示ErbB4激酶活性與傷害性熱刺激感受有關(guān)。為了進一步驗證這一點,作者對敲入突變株的T796G小鼠進行了研究,在T796G小鼠中,ErbB4可以被體積較大的抑制劑1NMPP1特異性抑制。鞘內(nèi)注射1NMPP1可降低脊髓腰膨大中pErbB4的表達。在行為反應(yīng)測試中,1NMPP1顯示了類似阿法替尼的效果。總之,這些結(jié)果表明脊髓中ErbB4的激酶活性與傷害性熱刺激感受有關(guān)。6. DRG中的NRG1參與了傷害性熱刺激的感受為了確定傷害性熱刺激感受是否與內(nèi)源性NRG1有關(guān),小鼠被注射了ecto-ErbB4(一種NRG1中和肽)。鞘內(nèi)注射ecto-ErbB4可減少脊髓中的pErbB4表達,并且增加小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期,減少辣椒素引起的舔足,但不會影響對針刺、掐和Von-Frey刺激的反應(yīng)。這些結(jié)果表明,內(nèi)源性NRG1參與了傷害性熱刺激的感受。NRG1在DRG中大量表達,為了確定DRG神經(jīng)元中的NRG1是否參與熱感覺,作者構(gòu)建了advillin-CreER;NRG1f/f小鼠,通過給予他莫西芬,可以誘導(dǎo)小鼠感覺性神經(jīng)節(jié)中NRG1的條件性敲除(cKO)。與對照相比,cKO小鼠脊髓中的NRG1和pErbB4蛋白的表達均減少,NRG1 mRNA的水平在DRG中降低,但在脊髓中沒有顯著變化。cKO小鼠在熱板和哈格里夫斯實驗中的反應(yīng)潛伏期增加,在辣椒素實驗中的舔足次數(shù)減少。然而,脊髓中的NRG1敲低對熱刺激行為反應(yīng)或背角中的pErbB4幾乎沒有影響。這些結(jié)果表明DRG中的NRG1信號在傷害性熱刺激的感受中起作用。7. NRG1-ErbB4信號能夠調(diào)控ErbB4+神經(jīng)元谷氨酸的傳遞上述結(jié)果已經(jīng)證明,表層中c-Fos+ ErbB4+神經(jīng)元大部分是興奮性神經(jīng)元。為了確定NRG1和ErbB4是否能夠調(diào)節(jié)谷氨酸的傳遞,作者將AAV-DIO-ChR2-EYFP病毒注射到ErbB4::CreER;Ai9小鼠中,在ErbB4+神經(jīng)元中特異性表達ChR2。在脊髓切片中,通過光刺激激活這些表達ChR2的ErbB4+神經(jīng)元,并在其鄰近的ErbB4-神經(jīng)元中記錄突觸后電流(PSCs)。在記錄的112 個ErbB4-神經(jīng)元中,當(dāng)膜電位鉗制在-70 mV時,其中31個神經(jīng)元記錄到了光刺激誘發(fā)的內(nèi)向電流;當(dāng)膜電位為0 mV時,所有神經(jīng)元均未記錄到光刺激誘發(fā)的外向電流,表明這些電流是EPSCs,而不是IPSCs。這些結(jié)果表明,表層的ErbB4+神經(jīng)元通過谷氨酸傳遞與下游神經(jīng)元進行交流。事實上,這些EPSCs能夠被AMPA受體和NMDA受體抑制劑CNQX和AP-5阻斷。根據(jù)這些EPSCs對TTX和4-AP的潛伏期和阻抗,可以確定,半數(shù)下游神經(jīng)元接受ErbB4+神經(jīng)元的單突觸神經(jīng)支配。用生物素標(biāo)記這些記錄神經(jīng)元的形態(tài)特征也支持這一觀點。接下來,作者確定了ErbB4+神經(jīng)元和靶細胞之間的谷氨酸傳遞是否受到NRG1-ErbB4信號通路的調(diào)控。在給予NRG1后的15分鐘內(nèi),光刺激誘發(fā)的EPSCs的波幅顯著增加,而這種作用在洗脫后減弱,表明NRG1促進谷氨酸傳遞。此外,給予ErbB4抑制劑阿法替尼降低了EPSC幅值,表明ErbB4激酶活性的參與谷氨酸傳遞。總之,這些數(shù)據(jù)證明了NRG1-ErbB4信號通路在脊髓谷氨酸傳遞中的作用。8. NRG1-ErbB4信號通路參與病理性的熱痛過敏在周圍神經(jīng)炎癥或損傷等病理條件下,機體對熱刺激的反應(yīng)更加敏感。在完全弗氏佐劑(Complete Freund’s Adjuvant, CFA)引起炎癥性疼痛模型中,小鼠患肢在哈格里夫斯實驗中的反應(yīng)潛伏期顯著降低。以下證據(jù)能夠表明NRG1-ErbB4信號通路在炎癥引起的熱痛過敏中起作用。首先,NRG1和pErbB4在CFA注射小鼠的同側(cè)脊髓腰膨大中的表達增加。第二,在哈格里夫斯實驗中,鞘內(nèi)中和NRG1能夠增加小鼠撤足的潛伏期。第三,阿法替尼能夠抑制野生型小鼠的熱痛過敏,1NMPP1能夠抑制T796G小鼠的熱痛過敏。此外,作者還研究了該通路在慢性壓迫性損傷(Chronic Constriction Injury, CCI)誘導(dǎo)的熱痛過敏反應(yīng)中的潛在作用。CCI能夠誘導(dǎo)小鼠在哈格里夫斯實驗中的反應(yīng)潛伏期降低,提示發(fā)生熱痛過敏。與假手術(shù)小鼠相比,CCI組小鼠同側(cè)腰膨大中NRG1和pErbB4的表達升高。野生型鞘內(nèi)給予ecto-ErbB4、阿法替尼、或T796G小鼠給予1NMPP1均可降低CCI引起的熱痛過敏。這些結(jié)果支持NRG1-ErbB4信號通路參與病理性的熱過敏的觀點。總結(jié)該研究通過分析熱刺激感受神經(jīng)元,識別出脊髓背角表層ErbB4在傷害性熱刺激的感受中發(fā)揮了關(guān)鍵作用。這些ErbB4+神經(jīng)元顯示以下特性。首先,它們主要接收來自攜帶傷害性信息的Aδ和C纖維的單突觸傳入,而不是接受來自攜帶非傷害性信息的Aβ纖維傳入。其次,ErbB4+神經(jīng)元受DRG中TRPV1+傷害性傳入纖維的單突觸支配,對傷害性熱刺激反應(yīng)較好,而對機械刺激反應(yīng)較差。第三,消融或抑制ErbB4+神經(jīng)元減弱了動物在熱板、哈格里夫斯以及辣椒素實驗中的反應(yīng),表明它們的活動與傷害性熱刺激的感受有關(guān)。最后,文章證明了NRG1-ErbB4信號通路在生理條件下的傷害性熱刺激感受和病理條件下的熱痛過敏反應(yīng)中的作用。亮點研究方法這項工作闡述了脊髓ErbB4+神經(jīng)元在傷害性熱刺激感受中的作用機制。研究用到了動物手術(shù)造模、行為學(xué)評估、光遺傳學(xué)、電生理記錄、組織病理檢測、給藥以及分子檢測等實驗技術(shù)。瑞沃德深耕生命科學(xué)研究領(lǐng)域20年,一直致力于為客戶提供可信賴的解決方案和服務(wù),可提供該研究中涉及的動物手術(shù)造模、行為學(xué)評估、光遺傳學(xué)、電生理記錄、組織病理檢測、給藥以及分子檢測等實驗的完整解決方案。截至目前,瑞沃德產(chǎn)品及服務(wù)覆蓋海內(nèi)外 100 多個國家和地區(qū),客戶涵蓋700+醫(yī)院,1000+科研院所,6000+高等院校,已助力科研人員發(fā)表SCI文章12000+,獲得行業(yè)廣泛認可。原文鏈接:https://doi.org/10.1016/j.neuron.2022.04.021
272人看過
- 2023-06-21 13:55:48《Small》:精確調(diào)控樣品磁性!氦離子輻照改善磁疇壁動力學(xué)
- 近年來,人們在不斷探索新型低能耗,高存儲密度的新型磁存儲材料。特別是對于磁疇壁動力學(xué)、斯格明子等方面的研究吸引了大批科研人員的目光。隨著研究的深入,制備出具有特定磁各項異性的材料并且進行精細的調(diào)控變的尤為重要。在對樣品特性精細調(diào)控的技術(shù)中,利用氦離子輻照是對樣品無損壞的一種高精度手段。氦離子輻照具有精度高、均勻性好、條件更加靈活、易于控制等優(yōu)勢,與其它改性方法相比,有利于器件或集成電路的大規(guī)模生產(chǎn)。基于此,法國Spin-Ion 公司經(jīng)多年研發(fā)推出離子輻照磁性精細調(diào)控系統(tǒng)Helium-S?。該系統(tǒng)采用創(chuàng)新的離子束技術(shù),可以通過超緊湊和快速的氦離子束設(shè)備精確控制原子間的位移,使其能夠在原子尺度上加工材料,并通過離子束工藝來調(diào)控薄膜和異質(zhì)結(jié)構(gòu)。設(shè)備一經(jīng)推出,便受到廣大科學(xué)家的關(guān)注,截止目前已有20多家科研和工業(yè)用戶以及合作伙伴使用該技術(shù),國內(nèi)也在北航和復(fù)旦等高校安裝該系統(tǒng),其獨有的技術(shù)正受到來自相關(guān)科研圈和工業(yè)領(lǐng)域越來越多的認可。 近期,來自于法國格勒諾布爾-阿爾卑斯大學(xué)CNRS-Institut Néel實驗室的Stefania Pizzini團隊聯(lián)合法國Spin-Ion Technologies公司的兩名工程師利用離子輻照磁性精細調(diào)控系統(tǒng)Helium-S?對Pt/Co/AlOx磁性薄膜進行了磁性調(diào)控研究。文章以“Improving Néel Domain Walls Dynamics and Skyrmion Stability Using He Ion Irradiation”為題發(fā)表在Small上。氦離子輻照量對樣品的磁各向異性的影響 文章討論了使用離子輻照磁性精細調(diào)控系統(tǒng)Helium-S?對Pt/Co/AlOx三層膜的磁性能產(chǎn)生的影響。研究人員發(fā)現(xiàn),氦離子輻照可以改善Néel磁疇壁的動力學(xué)和斯格明子的穩(wěn)定性。輻照可以降低垂直磁各向異性(PMA),而不影響界面Dzyaloshinskii-Moriya相互作用(DMI)的強度。這使得磁疇壁可以在較低的磁場下達到更大的速度。該研究表明,將PMA與DMI分離對于基于磁疇壁動力學(xué)的低能耗設(shè)備的設(shè)計是有益的。同時,輻照還可以調(diào)節(jié)斯格明子的大小和穩(wěn)定性,使其更加穩(wěn)定并且可以在更高的磁場下存在。這些結(jié)果表明氦離子輻照可以對基于磁疇壁動力學(xué)和斯格明子的低能耗設(shè)備的設(shè)計產(chǎn)生積極影響。氦離子輻照量對樣品的磁疇壁和斯格明子的影響 該項工作中使用的離子輻照磁性精細調(diào)控系統(tǒng)Helium-S?已經(jīng)成為磁性薄膜研究與性能調(diào)控的重要手段。該系統(tǒng)可以對直徑1英寸的晶圓進行掃描輻照,具有精度高,可控性好等特點。 應(yīng)用領(lǐng)域:? 磁性隨機存儲器(MRAM):自旋轉(zhuǎn)移矩磁性隨機存儲(STT-MRAM),自旋軌道矩磁性隨機存儲(SOT-MRAM),磁疇壁磁性隨機存儲(DW-MRAM)等;? 自旋電子學(xué):斯格明子,磁性隧道結(jié),磁傳感器等;? 磁學(xué)相關(guān):磁性氧化物,多鐵性材料;? 其他方向:薄膜改性,芯片加工,仿神經(jīng)器件,邏輯器件等。 產(chǎn)品特點:? 可通過超緊湊和快速的氦離子束設(shè)備精確控制原子間的位移,通過氦離子輻照可精確調(diào)控磁性薄膜或晶圓的磁學(xué)性質(zhì)。? 可提供能量范圍:1-30 keV的He+離子束? 采用創(chuàng)新的電子回旋共振(ECR)離子源? 可對25 mm的試樣進行快速的均勻輻照(幾分鐘)? 超緊湊的設(shè)計,節(jié)省實驗空間? 可與現(xiàn)有的超高真空設(shè)備互聯(lián)離子輻照磁性精細調(diào)控系統(tǒng)Helium-S? 測試數(shù)據(jù):調(diào)控界面各向異性性質(zhì)和DMI 低電流誘發(fā)的SOT轉(zhuǎn)換獲取 控制斯格明子和磁疇壁的動態(tài)變化 用戶單位 已經(jīng)購買該設(shè)備的國內(nèi)外用戶單位:Beihang University (China)Fudan University (China)University of California San Diego (USA)University of California Davis (USA)New York University (USA)Georgetown University (USA)Northwestern University (USA)University of Lorraine (France)SPINTEC Grenoble (France)University of Cambridge (UK)University of Manchester (UK)Nanyang Technological University (Singapore)A*STAR (Singapore)University of Gothenburg (Sweden)Western Digital (USA)IBM (USA)Singulus Technologies (Germany) 文章列表:[1]. Tailoring magnetism by light-ion irradiation, J Fassbender, D Ravelosona, Y Samson, Journal of Physics D: Applied Physics 37 (2004)[2]. Ordering intermetallic alloys by ion irradiation: A way to tailor magnetic media, H Bernas & D Ravelosona, Physical review letters 91, 077203 (2003)[3]. Influence of ion irradiation on switching field and switching field distribution in arrays of Co/Pd-based bit pattern media, T Hauet & D Ravelosona, Applied Physics Letters 98, 172506 (2011)[4]. Ferromagnetic resonance study of Co/Pd/Co/Ni multilayers with perpendicular anisotropy irradiated with helium ions, J-M.Beaujour & A.D. Kent & D.Ravelosona &E.Fullerton, Journal of Applied Physics 109, 033917 (2011)[5]. Irradiation-induced tailoring of the magnetism of CoFeB/MgO ultrathin films, T Devolder & D Ravelosona, Journal of Applied Physics 113, 203912 (2013)[6]. Controlling magnetic domain wall motion in the creep regime in He-irradiated CoFeB/MgO films with perpendicular anisotropy, L.Herrera Diez & D.Ravelosona, Applied Physics Letter 107, 032401 (2015)[7]. Measuring the Magnetic Moment Density in Patterned Ultrathin Ferromagnets with Submicrometer Resolution, T.Hingant & D.Ravelosona & V.Jacques, Physical Review Applied 4, 014003 (2015)[8]. Suppression of all-optical switching in He+ irradiated Co/Pt multilayers: influence of the domain-wall energy, M El Hadri & S Mangin & D Ravelosona, J. Phys. D: Appl. Phys. 51, 215004 (2018)[9]. Tuning the magnetodynamic properties of all-perpendicular spin valves using He+ irradiation, Sheng Jiang & D.Ravelosona & J.Akerman, AIP Advances 8, 065309 (2018)[10]. Enhancement of the Dzyaloshinskii-Moriya Interaction and domain wall velocity through interface intermixing in Ta/CoFeB/MgO, L Herrera Diez & D Ravelosona, Physical Review B 99, 054431 (2019)[11]. Enhancing domain wall velocity through interface intermixing in W-CoFeB-MgO films with perpendicular anisotropy, X Zhao & W.Zhao & D Ravelosona, Applied Physics Letter 115, 122404 (2019)[12]. Controlling magnetism by interface engineering, L Herrera Diez & D Ravelosona, Book Magnetic Nano- and Microwires 2nd Edition, Elsevier (2020)[13]. Reduced spin torque nano-oscillator linewidth using He+ irradiation, S Jiang & D Ravelosona & J Akerman, Appl. Phys. Lett. 116, 072403 (2020)[14]. Spin–orbit torque driven multi-level switching in He+ irradiated W–CoFeB–MgO Hall bars with perpendicular anisotropy, X.Zhao & M.Klaui & W.Zhao & D.Ravelosona, Appl. Phys. Lett 116, 242401 (2020)[15]. Magnetic field frustration of the metal-insulator transition in V2O3, J.Trastoy & D.Ravelosona & Y.Schuller, Physical Review B 101, 245109 (2020)[16]. Tailoring interfacial effect in multilayers with Dzyaloshinskii–Moriya interaction by helium ion irradiation, A.Sud & D.Ravelosona &M.Cubukcu, Scientific report 11, 23626 (2021)[17]. Ion irradiation and implantation modifications of magneto-ionically induced exchange bias in Gd/NiCoO, Christopher J. Jensen & Dafiné Ravelosona, Kai Liu, Journal of Magnetism and Magnetic Materials 540, 168479 (2021)[18]. Helium Ions Put Magnetic Skyrmions on the Track, R.Juge & D.Ravelosona & O.Boulle, Nano Lett. 2021 Apr 14;21(7):2989-2996參考文獻:[1]. Cristina Balan, Johannes W. van de Jagt, et al. Improving Néel Domain Walls Dynamics and Skyrmion Stability Using He Ion Irradiation. Small, 2023. https://doi.org/10.1002/smll.202302039
97人看過
- 2022-10-14 09:04:14直播回顧 |「大成學(xué)堂」DA(VTA)→5-HT(DRN)神經(jīng)環(huán)路調(diào)控神經(jīng)厭食癥
- 9月27日(周二)20:00,最/新一期「大成學(xué)堂」直播活動成功舉辦。本次直播,美國貝勒醫(yī)學(xué)院劉海蘭博士在線詳解神經(jīng)性厭食癥新調(diào)控機制的前沿研究。該研究成果已發(fā)表在Nature Neuroscience上,題為“A D2 to D1 shift in dopaminergic inputs to midbrain 5-HT neurons causes anorexia in mice”。作為第 一作者,劉海蘭博士在此次直播中細致講解了其研究的思路,并在線解答了大家的提問,獲得滿屏好評。沒有趕上看直播或想再回顧精彩內(nèi)容的小伙伴掃碼即可查看直播回放首先,劉海蘭博士介紹了研究背景。神經(jīng)性厭食癥作為一種高致死的精神疾病,近年來發(fā)病率顯著上升,但是其發(fā)病機制并不明確、治 療手段也有限。目前基礎(chǔ)研究和臨床研究表明,神經(jīng)性厭食癥的病人伴隨著多巴胺受體的多位點突變,這提示多巴胺神經(jīng)系統(tǒng)的異常也與厭食癥的發(fā)生 發(fā)展有關(guān)。同時研究表明位于中腦腹側(cè)被蓋區(qū)(VTA)的多巴胺(dopamine)神經(jīng)元和位于中腦中縫背核(DRN)的五羥色胺(5-HT)神經(jīng)元能夠參與調(diào)控包括進食在內(nèi)的動機性行為,它們也被發(fā)現(xiàn)與神經(jīng)性厭食癥的發(fā)病機制相關(guān)。基于這些研究背景,隨后劉海蘭博士分享了研究的詳細情況。其團隊利用TPH2-CreER小鼠模型開展了系列實驗,采用神經(jīng)環(huán)路示蹤技術(shù)和電生理技術(shù),首次發(fā)現(xiàn)了中腦腹側(cè)被蓋區(qū)-中縫背核(VTA→DRN)的DAVTA神經(jīng)元→5-HTDRN神經(jīng)元環(huán)路調(diào)控食欲和神經(jīng)性厭食癥。主要研究過程,主要為以下四方面內(nèi)容:低頻刺激抑 制DAVTA→5-HTDRN神經(jīng)環(huán)路并通過 DRD2 促進攝食行為高頻刺激激活DAVTA→5-HTDRN神經(jīng)環(huán)路并通過 DRD1 抑 制攝食行為DAVTA→5-HTDRN神經(jīng)環(huán)路的活動調(diào)控神經(jīng)厭食癥5-HTDRN神經(jīng)元中的 DA受體可調(diào)節(jié)神經(jīng)厭食癥狀直播時觀眾們提問踴躍,但是由于時間限制無法一一解答。在這里,我們特意整理出部分提問文字版的解答~聊天區(qū)部分問題詳解(文字版)1.研究神經(jīng)性厭食癥除了常見的轉(zhuǎn)基因技術(shù)、電生理技術(shù)之外,是否有新的實驗方法能嘗試?答:在我們的課題中除了用了電生理,以及這些轉(zhuǎn)基因小鼠模型之外,我們也使用了化學(xué)遺傳學(xué)、光遺傳學(xué)方法去慢性或急性的操控神經(jīng)元的活性,同時我們也使用了光纖記錄,實時記錄神經(jīng)元的活性改變。2.aba小鼠的成功率和存活率有多少?答:在這個過程中我們的那個存活率,因為我們這邊動物protocal上限制的是如果小鼠的體重低于原始體重的80%,就必須要處死,所以我們算存活率是當(dāng)小鼠體重降到它原來體重的80%的時候,我們就認為這只動物已經(jīng)死了。所以在我們的aba模型中,通常到第三天左右就會有動物的體重低于原來體重的80%,然后隨著到第四天第五天可能會有50%左右的小鼠體重低于80%。3.激活DRN中5HT神經(jīng)元如何能減少進食?答:5-HT神經(jīng)元它在攝食中的作用已經(jīng)有很多報道了。有一些報道說5-HT神經(jīng)元可以投射至下丘腦的POMC和AgRP神經(jīng)元。POMC和AgRP神經(jīng)元在攝食中的作用也是被許許多多研究證實的。POMC神經(jīng)元它可以抑 制AgRP神經(jīng)元,激活食欲。而5-HT神經(jīng)元可以通過它的受體抑 制AgRP神經(jīng)元,同時激活POMC神經(jīng)元活性來抑 制食欲。想觀看本期全程回放識別下方二維碼即可收看「大成學(xué)堂」以建立“全 球精英分享先進技術(shù),解析領(lǐng)域內(nèi)研究熱點”為宗旨的知識分享平臺。欄目開播以來已開展了超10場直播活動,數(shù)十名海內(nèi)外知名學(xué)者在此講授生命科學(xué)學(xué)術(shù)理論、實驗技術(shù)等課程。歡迎大家進入「大成學(xué)堂」專題頁,學(xué)習(xí)相關(guān)課程。?掃碼入群,提前獲取后續(xù)直播課信息以及get到豐富的學(xué)術(shù)干貨~
231人看過
- 2022-05-30 14:47:07直播回放|炎性小體在創(chuàng)傷性腦損傷后的調(diào)控機制研究進展
- 5月12日,「大成學(xué)堂」特邀邁阿密大學(xué)米勒醫(yī)學(xué)院 Dr. Juan Pablo de Rivero Vaccari為大家?guī)碇黝}為“炎性小體在創(chuàng)傷性腦損傷后的調(diào)控機制研究進展”的精彩直播講座。Dr. Pablo結(jié)合基礎(chǔ)研究與臨床研究,全面分享了創(chuàng)傷性腦損傷后炎癥小體的研究!沒來得及看現(xiàn)場直播的小伙伴們,現(xiàn)在福利來啦~直播回放掃碼回看Dr. Pablo致力于邁阿密大學(xué)米勒醫(yī)學(xué)院&邁阿密癱瘓治療項目,作為神經(jīng)外科研究副教授,從事先天免疫反應(yīng)研究超過15年,是首位證明炎性小體在體內(nèi)參與無菌性炎癥的科學(xué)家。講座干貨滿滿,小沃先來給大家劃個重點~在嚙齒動物和人類發(fā)生創(chuàng)傷性腦損傷后,炎性小體在先天免疫反應(yīng)中發(fā)揮著重要作用;小膠質(zhì)細胞中的炎性小體在TBI后的炎性反應(yīng)中起到了重要的促進作用;炎性小體是TBI的可靠生物標(biāo)志物;炎性小體在中 樞神經(jīng)損傷患者的細胞外囊中升高,并在TBI后促進了系統(tǒng)性炎癥的發(fā)生。想獲取更詳細的內(nèi)容掃描下方二維碼,快來觀看直播回放吧
215人看過




