百年細胞治療史,CAR-T未來如何突破?
2021 年是中國細胞 治 療領域的元年,時至今日,6 款產品獲得 FDA 批準,3 款在中國上市。基于已發布的 2022 年上半年財報[1-4],CAR-T 細胞治 療全 球總銷售額已超 10 億美金。

CAR-T 細胞制備流程包括以下幾個步驟:
① 抽取血樣,白細胞分離;
② 在 GMP 環境下,準備 CAR 基因,進行 CAR 基因轉導,獲取 CAR-T 細胞
③ CAR-T 細胞擴增,純化,并進行質量控制檢查;
④ 運送回治 療機構,病人先進行淋巴細胞清除化療,再輸注 CAR-T;
⑤ CAR-T 細胞識別并殺傷癌細胞。
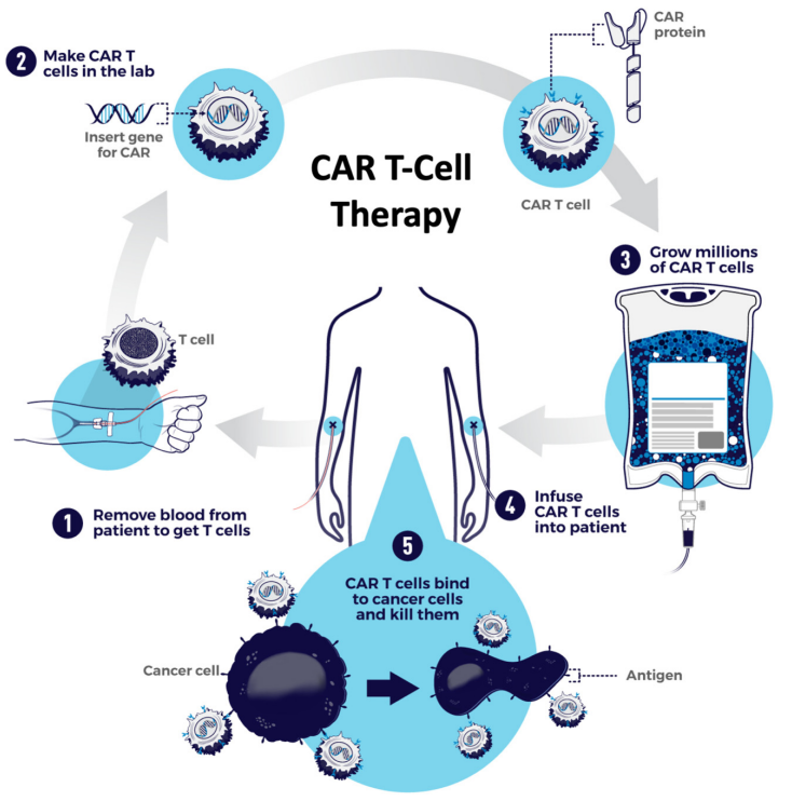
Cancers 2021, 13, 5181(原始圖來自于 NCI-NIH)[5]
點擊查看 CAR-T 細胞療法研發與生產解決方案


血液腫瘤
CAR-T 細胞治 療,徹底改變了血液系統惡性腫瘤的治 療結果。CD19 CAR-T 臨床適應癥主要為難治性大 B 細胞淋巴瘤、濾泡性淋巴瘤、急性淋巴細胞性白血病等,BCMA CAR-T 則針對多發性骨 髓瘤。
CAR-T 總體反應率在 52-85%,完全應答率達到 33-59%[5-7],優于單克隆抗體藥物(如Tafasitamab)、小分子抑 制劑(如Selinexor)、ADC 藥物(如Polatuzumab vedotin)等。
目前 FDA 已經批準了六款 CAR-T 細胞治 療產品,具體數據參考下表。
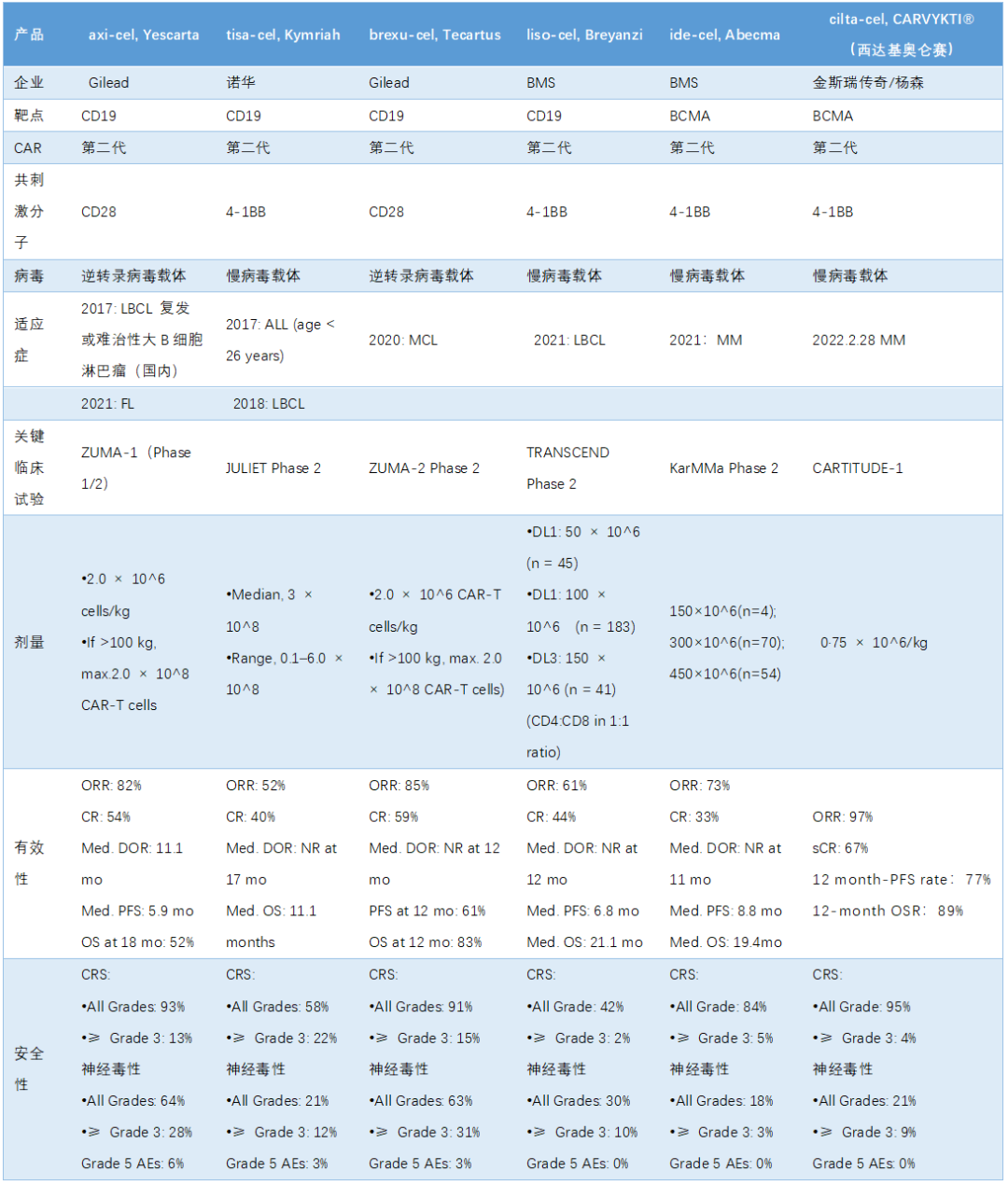
實體瘤
針對實體瘤(如肝細胞癌、胃癌、黑色素瘤、前列腺癌、卵巢癌等),目前雖然進行了數百項 CAR-T 臨床研究,比如 Mesothelin(29 項),HER2 和 GD(各 26 項),GPC3(23 項)CEA 和 CLDN 18.2(各 10 項),除去 CLDN 18.2(科濟 CT041)取得 ORR 48% 的療 效,其余靶點大多無應答[8]。

一. 可及性
目前 CAR-T 細胞治 療依然采用個體化生產,產能有限、生產周期長,且成本高昂,影響患者可及性。
二. 治 療相關副作用
作為免疫治 療產品,CAR-T 存在免疫相關一些副作用,包括細胞因子風暴(CRS)和神經毒性等,如上表統計 6 已經上市產品[5-7]。此外,脫靶毒性等也是不能忽略的問題。
三. 原發性耐藥
部分腫瘤細胞對于 CAR-T 治 療不敏感,無法產生消退。
四. 復發問題
從長時間看,細胞治 療產生消退的患者,如多發性骨 髓瘤 50% 以上會復發(無進展生存期小于 12 個月)[7]。
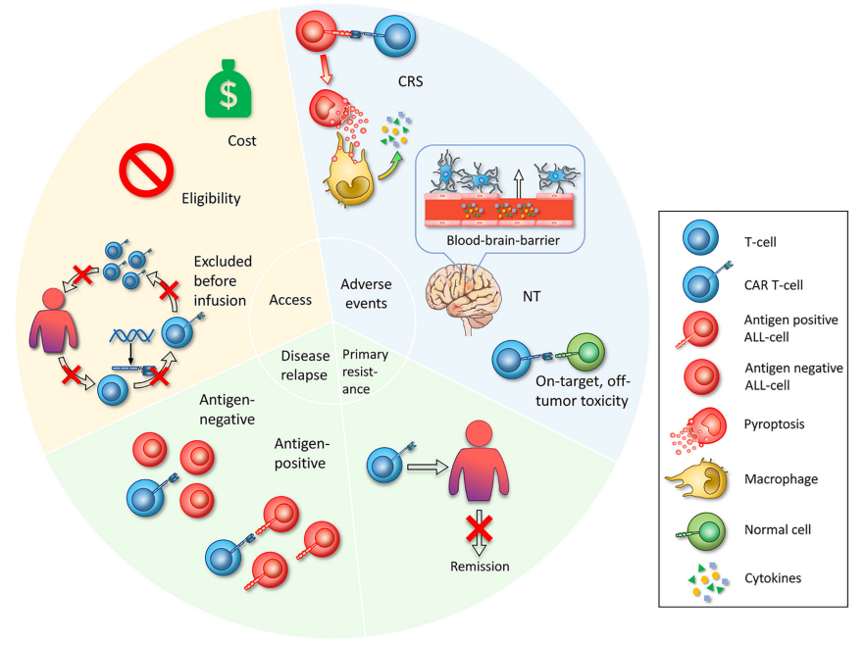
CAR-T 面臨的挑戰(Front. Immunol. 11:569117)[10]
五. 實體瘤
目前 CAR-T 治 療實體瘤,應答率和有效率都極低,相關機制討論中,涉及缺乏特異性腫瘤相關抗原,物理屏障阻隔 CAR-T 穿透入實體瘤內部,惡劣的腫瘤微環境誘導 CAR-T 功能耗竭等。
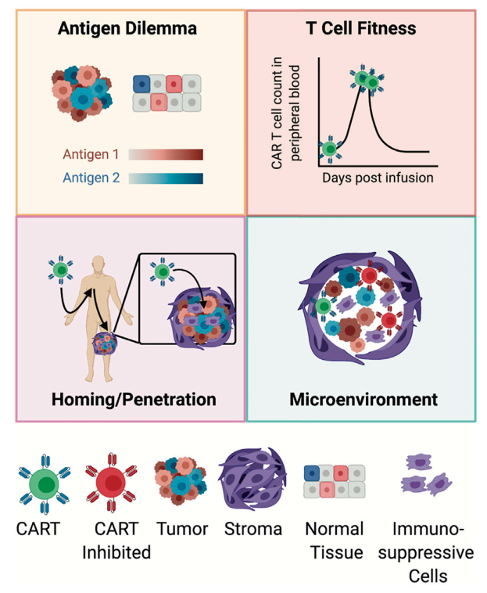
Molecular Therapy (2020)
除了以上挑戰之外,CAR-T 細胞的質量控制,臨床前試驗模型的缺乏等也是研發和臨床申報中廣泛面臨的問題。

一. 現貨型 CAR-T 解決可及性問題
現貨型 CAR-T 的優勢:
1. 可提前制備,直接使用;
2. 可批量生產,降低成本;
3. 產品質量與患者個體狀況無關。
現貨型 CAR-T 的開發策略:
宿主同種異體 T 細胞識別未修飾 T 細胞上不匹配的人類白細胞抗原(HLAs),引起排斥反應。一些宿主 NK 細胞也可能感覺到不匹配的 T 細胞上某些宿主 HLAI 類分子的缺乏,促進排斥。現貨型 CAR-T 主要開發邏輯是阻斷移植排斥反應。
常用的策略包括:
▲ 敲除引起移植排斥反應的 HLA 分子;
▲ 過表達 HLA-E/G 或 CD47;
▲ 在現貨型 CAR-T 細胞上保留 HLA-C 和非經典的 HLAI 類分子;
▲ 主動的方法可以通過非選擇性抑 制宿主免疫(清除宿主淋巴細胞,包括 CD52/CD38 單克隆抗體和 FOLFOX);
▲ 選擇性消除激活的同種異體反應性淋巴細胞。
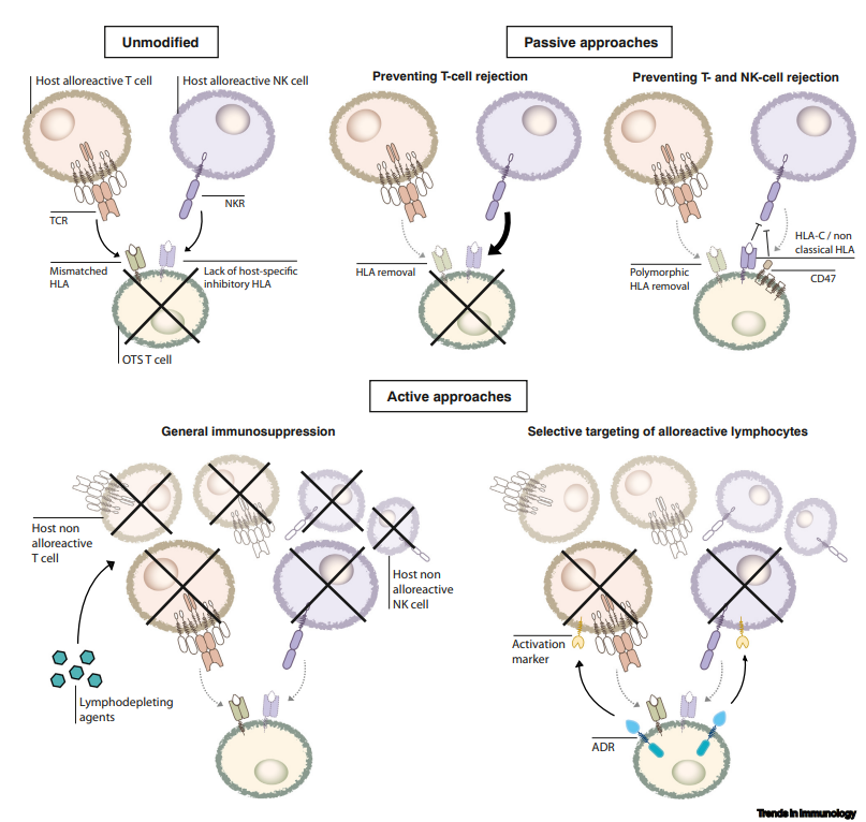
現貨 CAR-T 開發策略[11]
但現貨型 CAR-T,基因敲除可能會引起 T 細胞染色體異常[13],存在安全性問題,該技術的先驅 Cellectis 和 Allogene 多次被叫停臨床研究。
二. CAR-M、CAR-NK 等多種 CAR 細胞
除了 CAR-T 之外,使用 CAR 武裝另外一個免疫效應細胞(NK 細胞)也成為研究熱點。CAR-NK 有多種優勢,比如對移植排斥反應天然抵抗,可以使用臍帶血干細胞分化產生 NK 細胞,因而天然具有現貨型 CAR 細胞的特征;體內半衰期短,可以降低毒副作用的考量。不過,現在只有 30 多個臨床開展,還沒有獲得令人振奮的臨床結果,開發尚需時間。
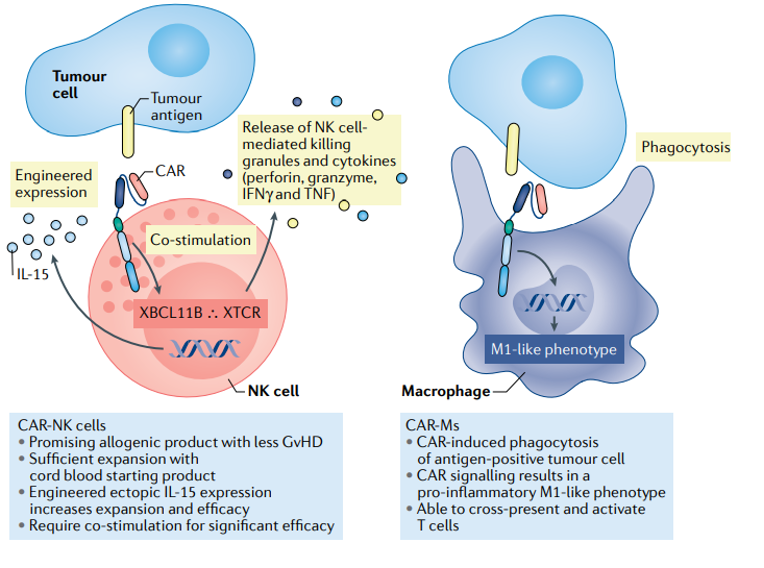
Nat Rev Cancer . 2021 Mar;21(3):145-161.[13]
CAR-M 巨噬細胞是抗原遞呈細胞,CAR-M 增加抗原遞呈能力,激活體內的 T 細胞,從而發揮抗腫瘤活性。但其臨床有效性也同樣需要時間來檢驗。
無論是 CAR 基因改造還是在多種 CAR 細胞中尋找最 優答案,都對操作環境、設備及操作符合規范的要求尤其嚴格。Eppendorf 系列產品不僅可以實現 CAR-T 細胞產品研發生產中的安全性、質量可控性、產品工藝一致性及數據合規性,更有高效節能和用戶友好的特點。
點擊圖片觀看網絡研討會:
高密度細胞培養技術
助力細胞治 療工藝產業化

點擊圖片觀看網絡研討會:
細胞治 療產品的工藝開發及產業化挑戰

CAR-T 在血液腫瘤驚艷的表現,讓 CAR-T 無疑成為人類攻克癌癥的重要武器。針對 CMC 研發生產的諸多困境,在通過現貨型 CAR-T 降低成本,增加可及性,通過基因工程改造 CAR 增加實體瘤穿透性的不同策略嘗試中,Eppendorf 將與您攜手共同探索發展與未來。
全部評論(0條)
推薦閱讀
-
- 百年細胞治療史,CAR-T未來如何突破?
- 作為免疫治 療產品,CAR-T 存在免疫相關一些副作用,包括細胞因子風暴(CRS)和神經毒性等,如上表統計 6 已經上市產品[5-7]。此外,脫靶毒性等也是不能忽略的問題。
-
- 百年史 | Brabender布拉本德百年歷史回顧
- 百年史 | Brabender布拉本德百年歷史回顧
-
- 深挖細胞治療:全球法規風暴下的創新技術突破與未來展望
- 8月13日,19:00-20:30
-

- 賽科成擺床反應器助力CAR-T細胞治療產品規模化擴增
- 細胞治療是對腫瘤患者或健康供者來源的免疫細胞于體外進行基因改造,賦予其腫瘤靶向性識別和殺傷能力,經體外擴增后將其回輸患者體內,對腫瘤發起精zhun、高效的攻擊,并可激活自身免疫系統對腫瘤的免疫應答。
-
- 直播預告 | 深挖細胞治療:全球法規風暴下的創新技術突破與未來展望
- 8月13日,19:00-20:30
-
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
-
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
-
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
- FDA重要通知解讀:CAR-T治療后的T細胞惡性腫瘤風險評估與優化前景
-

- 自體CAR-T細胞藥品供應鏈管理規范開始實施
- 10月13日,全國團體信息平臺發布了由上海醫藥行業協會和上海藥品審評核查中心組織起草的《自體CAR-T細胞藥品供應鏈管理規范》(T/SHPPA 011—2021)團體標準,該標準2021年10月18日起實施。
-

- CAR-T細胞載體拷貝數檢測的qPCR法考量
- CAR-T和TCR-T都屬于比較主流的特異性免疫細胞治療,且細胞來源相同,均來自外周血單核細胞(PBMC)、自體或同種異體細胞。
-
- 細胞治療新能手——細胞復蘇儀的時代來了!
- 重磅新品,順勢而生
-
- 下一代細胞治療生產平臺即將發布
- 基因藥物創新發布會\x0d\x0a7月3號正式開啟
-
- 讓創新落地-細胞治療產業化研討會
- 讓創新落地-細胞治療產業化研討會
①本文由儀器網入駐的作者或注冊的會員撰寫并發布,觀點僅代表作者本人,不代表儀器網立場。若內容侵犯到您的合法權益,請及時告訴,我們立即通知作者,并馬上刪除。
②凡本網注明"來源:儀器網"的所有作品,版權均屬于儀器網,轉載時須經本網同意,并請注明儀器網(www.ghhbs.com.cn)。
③本網轉載并注明來源的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點或證實其內容的真實性,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品來源,并自負版權等法律責任。
④若本站內容侵犯到您的合法權益,請及時告訴,我們馬上修改或刪除。郵箱:hezou_yiqi


























參與評論
登錄后參與評論